Les vétérinaires et les propriétaires sont souvent confrontés à des affections douloureuses chez le cheval, telles que des boiteries, la douleur abdominale, la douleur post-chirurgicale ou des douleurs plus chroniques. En fonction de l’origine et de l’intensité de la douleur, une seule molécule peut suffire mais une analgésie efficace peut aussi nécessiter une prise en charge multimodale. Dechra met à la disposition des vétérinaires une gamme complète, permettant de s’adapter à chaque patient.
L’Association Internationale pour l’Etude de la Douleur la définit comme “une expérience sensorielle et émotionnelle désagréable, associée à une lésion tissulaire avérée ou probable ». La douleur est un symptôme important de nombreuses conditions médicales et peut impacter la physiologie générale du cheval, sa performance ou sa qualité de vie. C’est l’une des raisons principales pour lesquelles les propriétaires font appel à leur vétérinaire ; mais elle peut être difficile à évaluer objectivement.
Il existe de nombreuses douleurs qui peuvent être classées selon leur origine, leur site, leur évolution,… Les douleurs fréquemment rencontrées chez le cheval incluent :
- Les boiteries (causes fréquentes d’origines variées : pied, membres et autres éléments de l’appareil musculo-squelettiques, dos ou encolure par exemple)
- Les douleurs abdominales (coliques)
- La douleur post-chirurgicale
- Les affections douloureuses oculaires ou dentaires
- Les affections dermatologiques douloureuses ou les plaies
Un traitement analgésique efficace repose sur :
1. Une bonne compréhension des mécanismes douloureux et des différentes étapes des voies de conduction de la douleur
2. Une détection et un suivi efficaces de la douleur
3. Des médicaments efficaces
Les étapes principales sont : la transduction, la transmission, la modulation et la perception. Le choix d’un traitement analgésique adapté dépend de l’identification de l’étape impliquée. En fonction de l’origine et de l’intensité de la douleur, une seule molécule peut suffire mais une analgésie efficace peut aussi nécessiter la combinaison de différentes molécules et/ou voies d’administration, qui ciblent différents récepteurs à différents niveaux de la conduction de la douleur afin d’établir une analgésie multimodale.
La transduction est l’étape à laquelle les stimuli nociceptifs sont convertis en signaux douloureux transmis par les nerfs périphériques au système nerveux central (SNC). Initialement un stimulus nociceptif est converti en signal électrique par l’activation de nocicepteurs des terminaisons nerveuses. Ces récepteurs sont sensibles à des stimuli thermiques, mécaniques ou chimiques.
Une hypersensibilisation périphérique peut apparaitre lorsque les médiateurs inflammatoires abaissent le seuil de douleur des nocicepteurs à proximité du site lésionnel.
Les molécules qui agissent sur la transduction :
- Les anesthésiques locaux (mépivacaine, lidocaine)
- Les opioïdes (butorphanol, buprénorphine)
- Les AINS (phénylbutazone, méloxicam (injectable ou oral), kétoprofène)
Le signal douloureux est ensuite transmis par le système nerveux sensitif (fibres nerveuses C et A-delta) à la corne dorsale de la moelle épinière via les nerfs périphériques afférents et le ganglion de la racine dorsale.
Les molécules qui agissent sur la transduction :
- Les anesthésiques locaux (mépivacaine, lidocaine)
Une fois que le signal a atteint la corne dorsale de la moelle épinière, il est modulé. La modulation des informations nociceptives a une influence considérable sur l’intensité de la douleur finalement ressentie par l’animal. Il existe des voies adrénergiques et sérotoninergiques descendantes entre le cerveau et la moelle épinière qui peuvent être activées et peuvent ensuite moduler le signal transmis par la moelle épinière. La modulation spinale affecte également la transmission du signal au cerveau et la façon dont il est finalement perçu par celui-ci. Si le système nerveux est stimulé de façon persistante par un stimulus nociceptif, il passe alors dans un état d’hyper réactivité, appelé sensibilisation centrale. Cela peut induire une diminution du seuil de douleur (hyperalgie) ou provoquer la perception d’une douleur provoquée par un stimulus non douloureux (allodynie). Les effets de la modulation spinale peuvent se prolonger pendant plusieurs heures, jours ou plus et peuvent être « inadaptés » à la gravité de la lésion initiale. Ce phénomène peut également conduire à l’installation d’une douleur chronique/neuropathique.
Les molécules qui agissent sur la modulation :
- Les anesthésiques locaux (mépivacaine, lidocaine)
- Les opioïdes (butorphanol, buprénorphine)
- Les AINS (phénylbutazone, méloxicam (injectable ou oral), kétoprofène)
- Les anesthésiques NMDA (kétamine)
- Les alpha-2 agonistes (détomidine, romifidine, xylazine (20 mg/ml ou 100 mg/ml))
Le signal transite par le cortex, le tronc cérébral et les centres nerveux supérieurs où la douleur est perçue. Jusqu’à ce que le signal atteigne le cortex, la douleur n’est pas perçue. Cependant, même chez un animal anesthésié qui ne manifeste pas sa douleur, les mécanismes nociceptifs sont présents. C’est pourquoi les réponses réflexes, telles que l’augmentation de la pression sanguine peuvent être observées en réponse à un stimulus chirurgical ; et une analgésie efficace (systémique ou locale) est essentielle même chez le patient anesthésié.
Les molécules qui agissent sur la perception :
- Les anesthésiques généraux (kétamine)
- Les opioïdes (butorphanol, buprénorphine)
- Les alpha-2 agonistes (détomidine, romifidine, xylazine (20 mg/ml ou 100 mg/ml))
La douleur physiologique est essentielle pour la survie et conditionne la détection et le réflexe de fuite face à une situation dangereuse. Ce type de douleur est bref et le retour à l’état physiologique est rapide.
La douleur clinique naît d’un traumatisme ou d’une inflammation et peut induire une sensibilisation persistante du système nociceptif.
La douleur neuropathique peut s’installer après un traumatisme direct du système nerveux lui-même ou à partir d’une réponse inflammatoire inadaptée et/ou persistante.
La douleur chronique peut se développer à partir d’une inflammation sévère ou d’une douleur neuropathique, provoquant parfois des modifications irréversibles du système nerveux et une résistance aux analgésiques.
La douleur doit donc être prise en charge afin de préserver le bien-être de l’animal, d’améliorer la convalescence et d’optimiser la réussite du traitement. (Bisgaard et al. 2001, Sellon et al. 2004)
Puisque la douleur est définie comme « une expérience sensorielle et émotionnelle désagréable », il peut être compliqué de l’évaluer de façon objective.
Jusqu’à présent, il n’existait pas d’échelle d’évaluation de la douleur. Ainsi, pour rendre cette évaluation aussi fiable que possible, il est important de déterminer les paramètres comportementaux et physiologiques associés à la douleur pour les observer de façon systématique, déterminer l’intensité de la douleur associée et les combiner afin d’établir un score quantitatif. Ce score peut être utilisé pour suivre l’évolution de la douleur et évaluer les besoins en analgésie.
Il existe plusieurs échelles de scoring de la douleur équine et elles sont généralement utilisées pour un type de douleur spécifique. Elles vont de la simple échelle descriptive à des échelles multi-paramètriques plus complexes. Lorsque c’est possible, il est préférable d’utiliser des échelles validées et adaptées au type de douleur rencontrée.
Exemples d’échelles d’évaluation de la douleur équine :
Echelle d’évaluation des boiteries de l’AAEP : de 0 à 5
Echelles d’évaluation multi-paramètriques :
- de la douleur orthopédique (Bussières et al. 2008)
- de la douleur viscérale postopératoire (Graubner et al 2011, van Loon et al.2014)
- de la douleur post-castration (échelle de l’UNESP-Botucatu, Taffarel et al. 2015)
Horse Grimace Scale (expressions faciales) :
- de la douleur post-castration (Dalla Costa et al. 2014)
- pour la fourbure aiguë (Dalla Costa et al. 2016)
- pour la douleur expérimentalement induite (The Equine Pain Face ; Gleerup et al. 2015)
EQUUS-FAP (Equine Utrecht University Scale for Facial Assessment of Pain = Echelle d’évaluation faciale de la douleur équine de l’Université d’Utrecht):
- des douleurs de la tête (van Loon and Van Dierendonck 2017)
- de la douleur viscérale aiguë (Van Dierendonck and van Loon 2016),
- pour la chirurgie orthopédique et les traumatismes (van Loon and Van Dierendonck 2019)
Les expressions faciales de la douleur ont été largement étudiées ces dernières années et constituent la base de plusieurs échelles d’évaluation validées et faciles à utiliser. Les chevaux peuvent afficher des expressions faciales facilement reconnaissables en lien avec la douleur. Par exemple, une position des oreilles basse, asymétrique ou légèrement en arrière, des yeux mi-clos ou des paupières « en accent circonflexe », une attitude prostrée, un regard fixe, des naseaux dilatés, un bout du nez tendu et des muscles de la mâchoire contractés. Certains comportements comme les mâchouillements, les bâillements, les grincements de dents ou le flehmen peuvent également être des manifestations de la douleur.
Lorsqu’on évalue la douleur, il est important de se référer à l’attitude « normale » du cheval ou de l’âne, et de se souvenir qu’examiner l’animal dans un environnement inhabituel (telle qu’une clinique) ou sous sédation peut biaiser cette évaluation. L’observation à distance ou sur vidéos peut être intéressante dans certaines circonstances. Les chevaux douloureux peuvent présenter des modifications de leur comportement général mais aussi présenter des comportements plus spécifiques de la douleur en cause. Par exemple, un report d’appui lié à une douleur orthopédique ; ou se regarder les flancs et se rouler en cas de colique. Les modifications du comportement général incluent : agitation, dépression, diminution de l’activité, perte d’appétit et diminution des interactions sociales.
Dès lors que le cheval présente une modification claire dans son attitude ou sa performance, une cause douloureuse doit être suspectée. Divers paramètres physiologiques ont été considérés historiquement pour évaluer l’intensité de la douleur. Cependant, les études ont montré que la corrélation est variable en fonction du type de douleur en cause. La mesure non invasive de la pression sanguine, la cortisolémie et les endorphines sanguines ont montré une bonne corrélation avec la douleur. Mais elles sont difficilement utilisables en pratique.
Une détection et un suivi fiables de la douleur sont essentiels à l’optimisation du traitement.
L’application EPWA a été développée par des chercheurs de la Faculté Vétérinaire d’Utrecht, pour faciliter la détection et le suivi de la douleur chez le cheval.
Conçue pour aider les vétérinaires et les propriétaires à améliorer le bien-être des chevaux, cet outil de diagnostic, simple et pratique, permet d’évaluer objectivement la douleur chez le cheval ou l’âne, grâce à une échelle d’évaluation multi-paramétrique ou à la reconnaissance des expressions faciales.
Dechra est fière d’avoir contribué à son développement.
L’application EPWA (Equine Pain and Welfare App = Application de la Douleur et du Bien-être Equins)

Présentation de l’application par le Dr Thijs van Loon (vidéo)
Découvrez ce que cette application peut apporter aux vétérinaires et aux propriétaires
Apprenez à évaluer la douleur des équidés grâce à l’application
Les AINS sont les molécules analgésiques les plus fréquemment utilisées chez le cheval. Leur action est surtout périphérique par inhibition des cyclo-oxygénases (COX-1 et COX-2), la diminution de la production d’eicosanoïdes dont les prostaglandines et les thromboxanes impliqués dans la réponse inflammatoire. Les AINS peuvent être administrés par voie orale et peuvent donc être utilisés pour le traitement de la douleur chronique. Sous forme injectable, ils peuvent être utilisés pour traiter la douleur aigüe ou péri-opératoire. Les AINS peuvent provoquer des effets indésirables rénaux ou gastro-intestinaux. Des AINS COX-2 spécifiques ou préférentiels ont été développés mais un bénéfice clinique net n’a pas encore été démontré.
Les AINS ayant une AMM chez le cheval en France sont :
- la phénylbutazone
- la flunixine méglumine
- le méloxicam
- le kétoprofène
Les opioïdes représentent le « gold-standard » de l’analgésie et peuvent également potentialiser les effets des sédatifs. Ils exercent leur action anti-nociceptive au niveau central principalement via les récepteurs mu, et leurs effets sédatifs s’exercent surtout via les récepteurs kappa. Les récepteurs opioïdes sont principalement situés dans le SNC, mais on peut aussi en trouver dans les tissus périphériques, comme les articulations par exemple. L’expression de ces récepteurs périphériques est affectée par l’inflammation. Les opioïdes agissent sur la modulation spinale et la commande cérébrale de la voie inhibitrice descendante, et peuvent donc contribuer à prévenir la sensibilisation centrale. Les opioïdes peuvent provoquer des effets indésirables tels qu’une diminution de la motilité intestinale et une augmentation de l’activité locomotrice ; ce qui a conduit certains praticiens à cesser d’utiliser ces puissantes molécules analgésiques. Les effets indésirables peuvent être, en général, facilement gérés et sont moins fréquemment observés chez les chevaux douloureux ou en association avec des sédatifs (tels que les alpha2-agonistes).
Les opioïdes ayant une AMM chez le cheval en France sont la buprénorphine et le butorphanol. La méthadone et la morphine n’ont pas d’AMM chez le cheval.
Les alpha-2 agonistes sont les piliers de la sédation chez le cheval. Les adrénorécepteurs sont situés dans la corne dorsale de la moelle épinière et agissent sur la voie inhibitrice descendante. Chaque alpha-2 agoniste possède sa propre durée d’action et sa propre sélectivité pour un récepteur alpha2.
Les alpha-2 agonistes ayant une AMM chez le cheval en France sont la xylazine (20 mg/ml ou 100 mg/ml), la détomidine et la romifidine.
Les anesthétiques locaux bloquent les canaux Na+ intracellulaires et ainsi la génération et la transmission d’un potentiel d’action, ce qui conduit à l’anesthésie des fibres sensitives. Les anesthésiques locaux peuvent être utilisés à des fins diagnostiques (boiteries par exemple) ou pour des procédures chirurgicales chez un animal sédaté ou anesthésié.
Les anesthétiques locaux ayant une AMM chez le cheval en France sont la mépivacaïne et la lidocaïne.
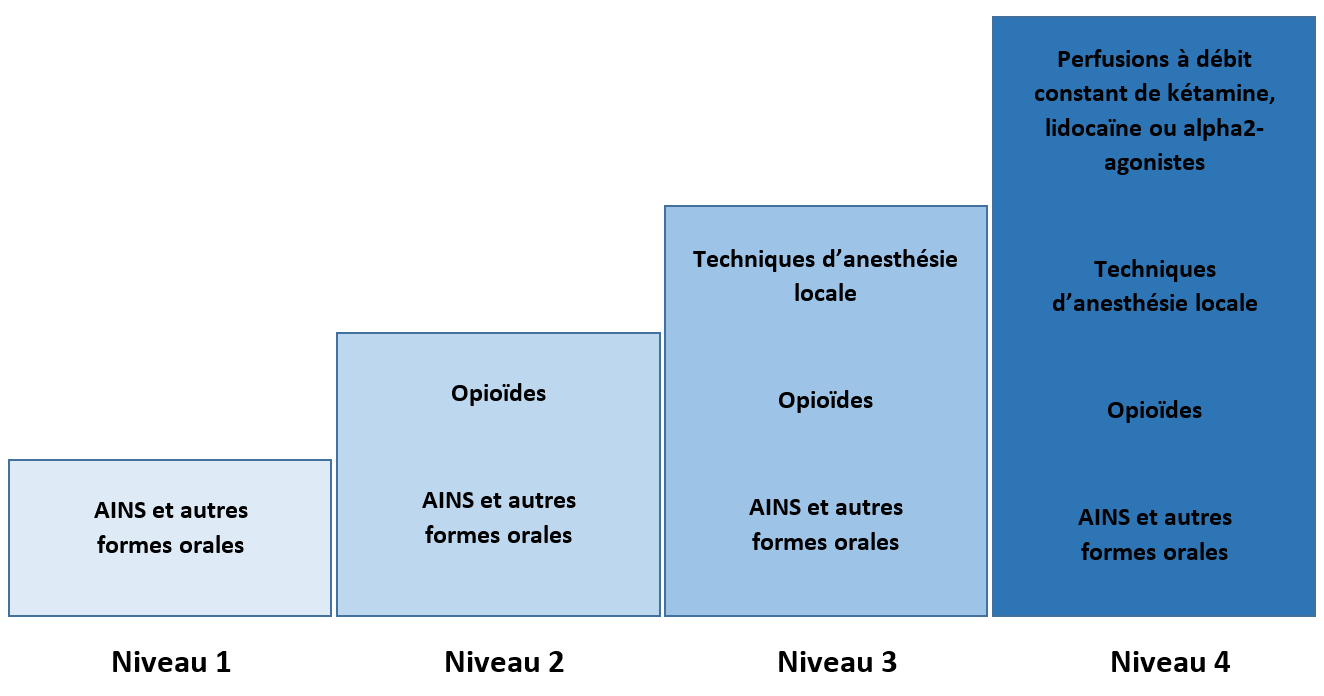
L’analgésie multimodale consiste à associer des molécules analgésiques qui ont des mécanismes d’action différents ou agissent à différents niveaux des voies de conduction de la douleur afin d’installer une analgésie de meilleure qualité, de réduire les doses de chaque produit et de diminuer les risques d’effets indésirables. Les effets sont synergiques ou au moins additifs. Par ex., les combinaisons d’opioïdes et d’AINS sont fréquemment utilisées en médecine vétérinaire.
Le choix d’un traitement analgésique adapté dépend de l’identification des processus douloureux impliqués. En fonction de l’origine et de l’intensité de la douleur, le recours à l’analgésie multimodale peut être un choix judicieux.
On sait que les chevaux peuvent réagir à des stimuli douloureux, même anesthésiés. On sait aussi qu’une analgésie insuffisante peut avoir une influence négative sur la période post-chirurgicale en termes de morbidité, mortalité, complications, durée d’hospitalisation et coûts de traitement ; dans les autres espèces et probablement aussi chez le cheval. Une prise en charge non adéquate de la douleur peut endommager le système nerveux, en provoquant par ex. une hyperalgésie ou une allodynie.
Nous devons garder à l’esprit que certaines molécules utilisées dans nos protocoles anesthésiques ont des propriétés analgésiques, comme les alpha2-agonistes, les AINS, la kétamine et les opioïdes, mais que d’autres en sont dépourvues, telles que l’acépromazine, le midazolam, le diazépam ou l’isoflurane. Un plan d’analgésie adapté inclura donc une analgésie en prémédication, et une analgésie intra- et post-opératoires. Une bonne analgésie péri-opératoire permet de faciliter l’entretien de l’anesthésie et le réveil, et d’augmenter de façon générale les chances de succès de la chirurgie.
Les techniques d’anesthésie régionale permettent d’effectuer de nombreux actes chirurgicaux sur cheval debout, d’éliminer ainsi les risques associés à l’anesthésie générale. Elles permettent également de réduire les doses de l’anesthésie générale, améliorant l’efficacité de l’analgésie et limitant les risques d’effets indésirables associés.
Références
Lerche, P and Muir, W. (2009) ‘Chapter 20. Perioperative Pain Management’ Equine Anesthesia: Monitoring and Emergency Therapy, Second Edition
Bisgaard,T; Kehlet. H. and Rosenberg, J. (2001) ‘Pain and convalescence after laproscopic cholecystectomy’ Eur. J. Surg. 167; pp. 84-96
Bussieres, G; Jacques, C; Lainey, O; Beauchamp, G; Leblond, A; Cadore, J.L; Desmaiziéres, L.M; Cuveilliez, S.G. and Troncy, E. (2008) ‘Development of a composite orthopaedic pain scale in horses’ Res. Vet. Sci. 85; pp. 294-306
Dalla Costa, E; Minero, M; Lebelt, D; Stucke, D; Canali, E. and Leach, M.C. (2014) ‘Development of the Horse Grimace Scale (HGS) as a pain assessment tool in horses undergoing routine castration’ PLoS One 19:9; pp. 3
Dalla Costa, E; Stucke, D; Dai, F; Minero, M; Leach, MC. and Lebelt, D. (2016) ‘Using the Horse Grimace Scale (HGS) to Assess Pain Associated with Acute Laminitis in Horses (Equus caballus)’ Animals 6(8)
Gleerup, K,B; Forkman, B; Lindegaard, C. and Andersen, P.H. (2015) ‘An equine pain face’ Vet Anaesth Analg. 42(1); pp. 103-14
Graubner, C; Gerber, V; Doherr, M. and Spadavecchia, C. (2011) ‘Clinical application and reliability of a post abdominal surgery pain assessment scale (PASPAS) in horses’ Vet. J. 188(2); pp. 178-183
Sellon, D.C; Roberts, M.C; Bilkslager, A.T; Ulibarri, C. and Papich. (2004) ‘Effects of continuous rate infusion of butorphanol on physiologic and outcome variables in horses after celiotomy’ J. Vet. Int. Med. 18; pp. 555-563
Taffarel, M.O; Luna, S.P; de Oliveira, F.A; Cardoso, G.S; Alonso, J. M; Pantoja, J.C; Brondani, J.T; Love, E; Taylor, P; White, K and Murrell, J.C. (2015) ‘Refinement and partial validation of the UNESP-Botucatu multidimensional composite pain scale for assessing postoperative pain in horses.’ BMC Vet. Res. 11; pp. 83
van Loon, JPAM. and Van Dierendonck, M.C. (2019) ‘Pain assessment in horses after orthopaedic surgery and with orthopaedic trauma’ Vet. J. 246; pp. 85-91
van Loon, J,P. and Van Dierendonck, M.C. (2017) ‘Monitoring equine head-related pain with the Equine Utrecht University scale for facial assessment of pain (EQUUS-FAP)’ Vet. J. 220; pp. 88-90
van Loon, J.P. and Van Dierendonck, M.C. (2015) ‘Monitoring acute equine visceral pain with the Equine Utrecht University Scale for Composite Pain Assessment (EQUUS-COMPASS) and the Equine Utrecht University Scale for Facial Assessment of Pain (EQUUS-FAP): A scale-construction study’ Vet. J. 206(3); pp. 356-364
van Loon, J.P; Jonckheer-Sheehy, V.S; Back, W; van Weeren, P.R. and Hellebrekers L.J. (2014) ‘Monitoring equine visceral pain with a composite pain scale score and correlation with survival after emergency gastrointestinal surgery’ Vet. J. 200(1); pp. 109-115
van Loon, J.P. (2014) ‘Multimodal strategies for equine analgesia, one step beyond. . .’ Equine vet. Educ. 26 (2); pp. 72-74